Tamiser un gaz radioactif pour séparer ses composants
Une collaboration entre le CEA - DAM et le laboratoire interdisciplinaire Carnot de Bourgogne vient de démontrer expérimentalement la complémentarité de deux effets pour séparer des isotopes de l’hydrogène par tamisage à l’échelle atomique : le premier dépend de la taille des molécules de gaz par rapport à celle du tamis ; le second implique des interactions fortes entre les molécules et le tamis [1]. Sur la base de ce résultat, le CEA - DAM vient de mettre en place ce procédé de purification du tritium, un isotope radioactif de l’hydrogène et une matière stratégique entrant dans la composition des armes nucléaires de la dissuasion française. Cette avancée permettra d’élaborer des matériaux qui rendront le procédé encore plus efficace.
Le tritium est un gaz radioactif qui possède des propriétés chimiques très voisines de celles de l’hydrogène. Cet isotope est un combustible de la fusion nucléaire, réaction qui alimente en énergie notre Soleil, mais aussi nos armes nucléaires. Avoir du tritium est une chose, en disposer avec une pureté suffisante en est une autre. Cette matière stratégique est purifiée et mise en œuvre dans le centre CEA - DAM de Valduc. Le procédé d’enrichissement du tritium génère comme sous-produit une fraction appauvrie en tritium, contenant majoritairement de l’hydrogène. Ce mélange de gaz contient trop peu de matière d’intérêt pour qu’elle soit valorisée, mais sa charge radioactive reste trop élevée pour qu’un rejet dans l’environnement soit conforme à la réglementation. Il est alors nécessaire de procéder à une ultime purification.
Le procédé de séparation existant est un processus qui nécessite de porter le gaz au contact d’un tamis moléculaire dans un environnement bien particulier, à une température de –233 °C. Le tamis est en zéolithe, un matériau extrêmement poreux, d’une surface interne de 600 m2 par gramme. Il est formé d’un assemblage de motifs se répétant à l’infini. Chacun d’eux contient une cage accessible par des ouvertures appelées fenêtres. Chaque fenêtre a une dimension caractéristique de 0,4 nanomètre, très proche de la taille apparente d’une molécule de gaz. Par ailleurs, la structure intègre dans la cage des ions qui jouent un rôle primordial. Ces ions apportent à la fois une modulation de la taille de la fenêtre et sont aussi à l’origine de fortes interactions électrostatiques avec les molécules d’hydrogène et de tritium.
L’amélioration des performances de ces matériaux est le principal levier pour réduire la taille du cryostat du procédé industriel, dispositif coûteux en ressources énergétiques et dont le dimensionnement croît exponentiellement avec la quantité de matériau à refroidir.
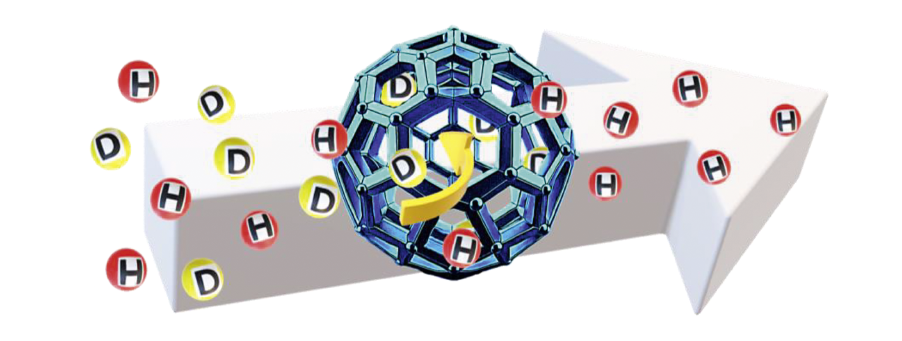
Le tritium étant radioactif, la mise au point de ce procédé est réalisée avec un isotope non radioactif de l’hydrogène, le deutérium. La recherche est donc menée dans un premier temps en laboratoire sur la séparation entre hydrogène et deutérium. Le gaz est refroidi à –233 °C afin d’optimiser la probabilité pour les molécules de pénétrer dans la cage et de permettre leur adsorption. En effet, l’agitation moléculaire est alors fortement réduite. À cette échelle atomique, on parle de tamisage quantique. Le principe est schématisé sur la figure 1.
Dans le cadre de nos travaux [1,2], deux ions différents sont positionnés dans une structure de zéolithe de type A : du lithium donnant le matériau noté Li-A, et du sodium donnant le matériau noté Na-A.
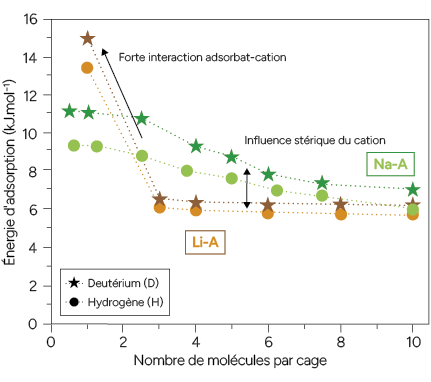
Grâce à ces ions, ces matériaux piègent environ dix fois plus de deutérium que d’hydrogène dans les cages de la zéolithe. Mais le type d’ion implanté a surtout permis de mettre en évidence deux phénomènes distincts suivant le remplissage, essentiels pour améliorer les performances de la purification. À faible remplissage (moins de deux molécules adsorbées par cage), les interactions électrostatiques (répulsives) entre les ions et les molécules sont prépondérantes et elles sont propres à la nature de l’ion. Sur la figure 2, le lithium présente une très forte interaction avec les molécules. À plus fort remplissage, l’ion est écranté par ces premières molécules, ce premier effet s’estompe. La sélectivité est alors gouvernée par la taille des fenêtres modulée par la présence d’ions plus ou moins volumineux. Les molécules de deutérium, plus petites que celles d’hydrogène, accèdent alors plus facilement aux cages. Le choix de l’ion est donc un paramètre clé pour l’élaboration de matériaux plus performants.
Ces travaux constituent une avancée vers le concept de matériaux plus efficaces pour la séparation du tritium. Ils contribueront à terme à l’amélioration du processus de traitement industriel pour le rendre plus performant. En parallèle, les études se poursuivent. Les données expérimentales acquises servent à alimenter des outils de simulation numérique. L’objectif est à terme de parvenir à prédire le comportement des tamis en fonction de leur structure et des ions. La réalisation d’expériences sera alors réservée aux matériaux identifiés numériquement comme les plus prometteurs, une manière bien plus efficace de réaliser le meilleur tamisage.
I. Bezverkhyy, V. Boyer, J.-P. Bellat Laboratoire interdisciplinaire Carnot de Bourgogne – UMR 6303 CNRS – Université de Bourgogne-Franche-Comté, Dijon
C. Cabaud CEA - DAM, centre de Valduc
figure 1
 Schéma de principe du tamisage quantique. Les molécules de gaz (H : hydrogène, D : deutérium) sont mises au contact du tamis (zéolithe) à une température de –233 °C. Seul le deutérium pénètre dans le matériau et s’adsorbe à la surface de la cage. L’hydrogène n’accède pas à l’intérieur et passe à côté du tamis. Dans un cas idéal, la séparation est totale.
Schéma de principe du tamisage quantique. Les molécules de gaz (H : hydrogène, D : deutérium) sont mises au contact du tamis (zéolithe) à une température de –233 °C. Seul le deutérium pénètre dans le matériau et s’adsorbe à la surface de la cage. L’hydrogène n’accède pas à l’intérieur et passe à côté du tamis. Dans un cas idéal, la séparation est totale.
figure 2
 Variation de l’énergie d’adsorption (de H ou D) pour Li-A et Na-A en fonction du remplissage d’une cage. À faible remplissage (moins de deux molécules par cage), l’interaction électrostatique est le mécanisme de séparation prépondérant. Elle est très marquée pour le lithium. À plus fort remplissage, l’ion Na+, plus gros, laisse préférentiellement l’accès au deutérium qui est de plus petite taille que l’hydrogène. Pour les deux mécanismes, l’adsorption du deutérium est favorisée et il en va donc de même pour le tritium.
Variation de l’énergie d’adsorption (de H ou D) pour Li-A et Na-A en fonction du remplissage d’une cage. À faible remplissage (moins de deux molécules par cage), l’interaction électrostatique est le mécanisme de séparation prépondérant. Elle est très marquée pour le lithium. À plus fort remplissage, l’ion Na+, plus gros, laisse préférentiellement l’accès au deutérium qui est de plus petite taille que l’hydrogène. Pour les deux mécanismes, l’adsorption du deutérium est favorisée et il en va donc de même pour le tritium.
références
1
I. Bezverkhyy, V. Boyer, C. Cabaud, J.-P. Bellat « D2/H2 separation by quantum sieving in LiNaA zeolites: the role of aperture size and strong guest-cation interactions », Adsorption, https://doi.org/10.1007/s10450-023-00425-8 (2023).
2
I. Bezverkhyy, M. Giraudet, C. Dirand, M. Macaud, J.-P. Bellat « Enhancement of D2/H2 selectivity in zeolite A through partial Na–K exchange: single-gas and coadsorption studies at 45-77 K », Journal of Physical Chemistry C, https://doi.org/10.1021/acs.jpcc.0c06902 (2020).

 Article précédent
Article précédent